التميز رؤى حول مكافحة كوفيد-19 من خلال التكرارات العنقودية المتناظرة القصيرة المنتظمة التباعد
مقدمة من معهد قطر لبحوث الطب الحيوي
تُعرف "التكرارات العنقودية المتناظرة القصيرة المنتظمة التباعد" اختصارًا بكريسبر "crisper"، وهي أحد الإنجازات الرئيسية ذات العلاقة بعلم الأحياء الجزيئي الحديث. في حلقة هذا الأسبوع، يشرح خبراء معهد قطر لبحوث الطب الحيوي كيف يمكن استخدام الجهاز المناعي البكتيري في علاج وتشخيص فيروس كورونا (كوفيد-19) لدى البشر.
تقنية كريسبر
اُستقبلت تقنية التكرارات العنقودية المتناظرة القصيرة المنتظمة التباعد (كريسبر) التي تُعالج الجينات، والمكتشفة مؤخرًا، بالترحاب لقدرتها الفائقة على تعديل الجينات. وتعتبر تقنية كريسبر في الواقع قاتلة للفيروسات الطبيعية، وقد اُكتشفت لأول مرة في بعض أنواع البكتيريا التي تحمي نفسها من العدوى الفيروسية، عن طريق تقطيع الحمض النووي الريبوزي الفيروسي إلى أجزاء، باستخدام "مقص جزيئي" يسمى بروتين (CRISPR/Cas).
ويعتبر الحمض النووي الريبوزي (RNA) جزيئًا بوليمريًا أساسيًا يتواجد ضمن المهام البيولوجية المتنوعة ذات العلاقة بتشفير الجينات وفك شفرتها وتنظيمها وطريقة عملها، والبروتين المرتبط بكريسبر (Cas) قادر على العثور على هدفه باستخدام "الحمض النووي الريبوزي الموجه"، الذي يقوده نحو المناطق التي تحمل المتواليات المماثلة. وقام الباحثون منذ ذلك الحين بتغيير متوالية الحمض النووي الريبوزي الموجه لإجراء التعديل الجيني على كائنات متعددة تشمل (حيوانات ونباتات وبشر وبكتيريا وفيروسات)، والتي يمكن أن يُستفاد منها في تطبيقات عديدة.
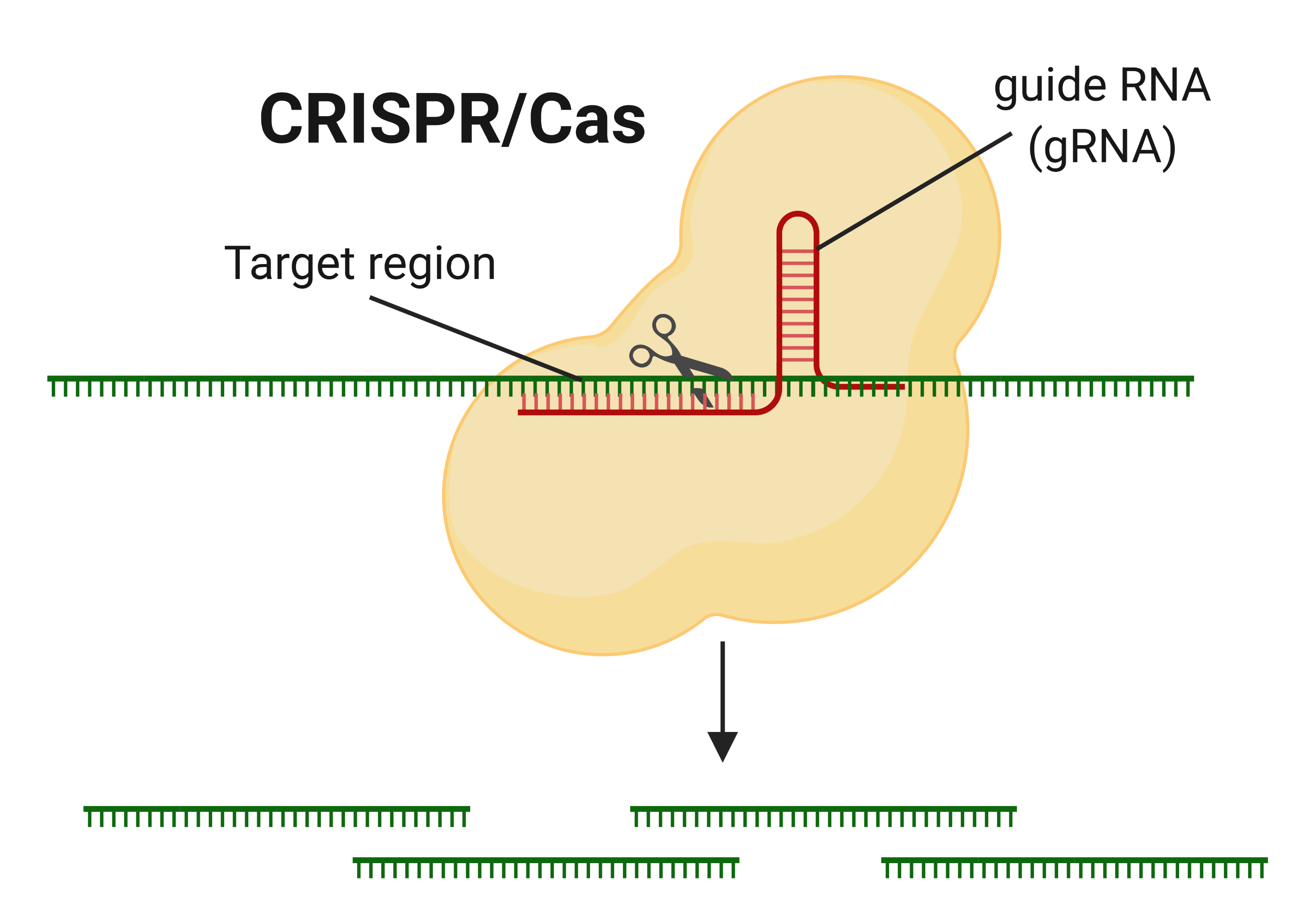
كريسبر لعلاج فيروس كورونا
بينما لا يزال العالم ينتظر التوصل إلى لقاح فعال ضد فيروس كورونا، يتوقع العلماء أن يستغرق هذه الأمر من 12 إلى 18 شهرًا على الأقل. وحتى الآن، لم تثبت الأدوية المُعاد استخدامها لأغراض أخرى حاليًا فاعلية مقنعة في مكافحة كوفيد-19. وقد أظهر عقار ريمديزيفير (Remdisivir)، وهو دواء فشل في علاج مرض الإيبولا، بعض العلامات التي تبشر بالنجاح مع المرضى في دراسة أُجريت في واشنطن بالولايات المتحدة الأمريكية، لكن من السابق لأوانه توقع فاعليته مع المرضى المصابين بسلالات متطورة من الفيروس. ومن جانب آخر، يتحور فيروس كوفيد-19 مثل باقي الفيروسات بشكل مستمر، ما يجعله أكثر قدرة على مقاومة الأدوية المضادة للفيروسات.
ومن خلال جهود مبتكرة، يبحث العلماء في الوقت الحالي طرقًا لعلاج كوفيد-19 باستخدام كريسبر، الذي قد يكون أكثر فاعلية من الأدوية واللقاحات التقليدية. وتعتمد معظم التجارب الجارية لانتاج لقاح لفيروس كورونا على "تدريب" نظام المناعة لدى الإنسان من خلال تعريضه لأجزاء من كوفيد-19 (مثل الشوكة الفيروسية أو بروتينات الغشاء). ونظرًا لأن فيروس كورونا في حالة تطور مستمر، ربما تكتسب السلالات المتحورة منه خصائص جديدة، تجعلها قادرة على تفادي رد الفعل المناعي. ولفهم أفضل لكيفية تخلص كريسبر من فيروس كورونا، نحتاج أن نلقي نظرة أولاً على كيفية إصابة الفيروس لخلايا الرئتين.
يستخدم كوفيد-19 بروتيناته "الشوكية" للهبوط على المستقبلات الموجودة على سطح خلايا الرئتين، ويدخل الخلية لإطلاق الحمض النووي الريبوزي الفيروسي، وهو ما يُعرف بالشفرة الوراثية لفيروس كورونا. وتحتوي هذه الشفرة على جميع المعلومات الضرورية لتكاثر الفيروس. ويستخدم الفيروس آلية خلايا الرئتين، التي تسمى الريبوزوم، وهو مصنع تكوين البروتين في الخلية، في قراءة شفرتها وترجمتها. يقرأ الريبوزوم جين (ORF1ab) لفيروس كورونا وينتج (RdRp)، وهو البروتين الوحيد الذي يمكنه قراءة بقية شفرة الحمض النووي الريبوزي الفيروسي لصنع مكونات جديدة للفيروس (من خلال عملية تسمى النسخ والتحويل) وينتج نسخ جديدة منه، وهو ما يُعرف بعملية (التكاثر). ومن السهل أن نرى الآن مدى أهمية الحمض النووي الريبوزي الفيروسي في بقاء وتكاثر فيروس كورونا في خلايا الإنسان، وقد يؤدي تدميره إلى كبح جماح الفيروس.
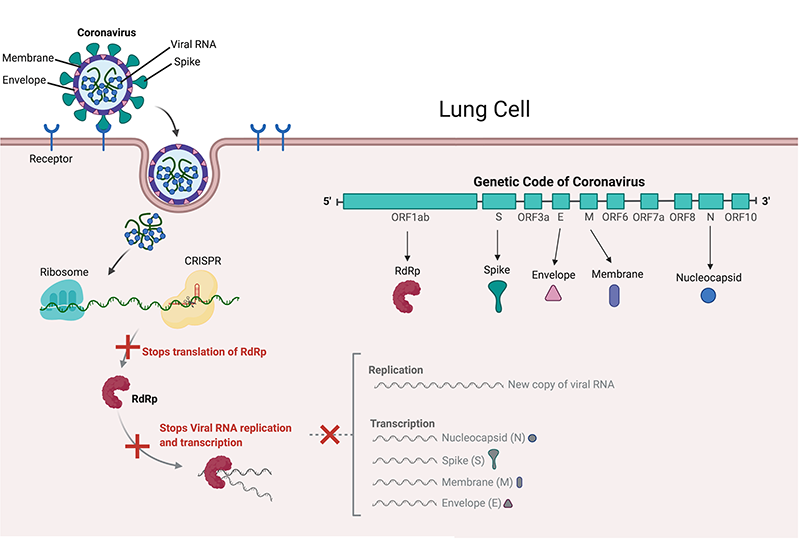
وقد تمكن فريقان من العلماء من العثور على الأجزاء غير المتطورة من شفرة الحمض النووي الريبوزي الفيروسي (المناطق المحفوظة) وتدميرها باستخدام كريسبر، كما استهدف فريق إيطالي يقوده الدكتور بيير باندولفي كريسبر "لمضغ" جيني (ORF1ab) و(S) لإيقاف فيروس كوفيد-19 من إنتاج (RdRp) وكذلك البروتينات الشوكية في خلايا الرئتين. واستهدف فريق الدكتور ستانلي كي في الولايات المتحدة جيني (ORF1ab) و(N)، اللذين ينتجان بروتينات نيوكليوكابسيد التي تحيط بالحمض النووي الريبوزي الفيروسي وتحميه.
من جهة أخرى، يمكن توسيع نفس المفهوم لاستهداف جينات أخرى مثل جينات (M) أو (E) التي تنتج غشاء وغلاف كوفيد-19. بالنظر إلى هذه الأهداف الشائعة بين الأدوية المضادة للفيروسات (يعمل عقار ريمديزيفير عن طريق تعطيل "RdRp)")، يوفر كريسبر ميزة من خلال قدرته على تدمير أهداف متعددة في نفس الوقت، ما يجعل من الصعب على فيروس كورونا الهروب منه.
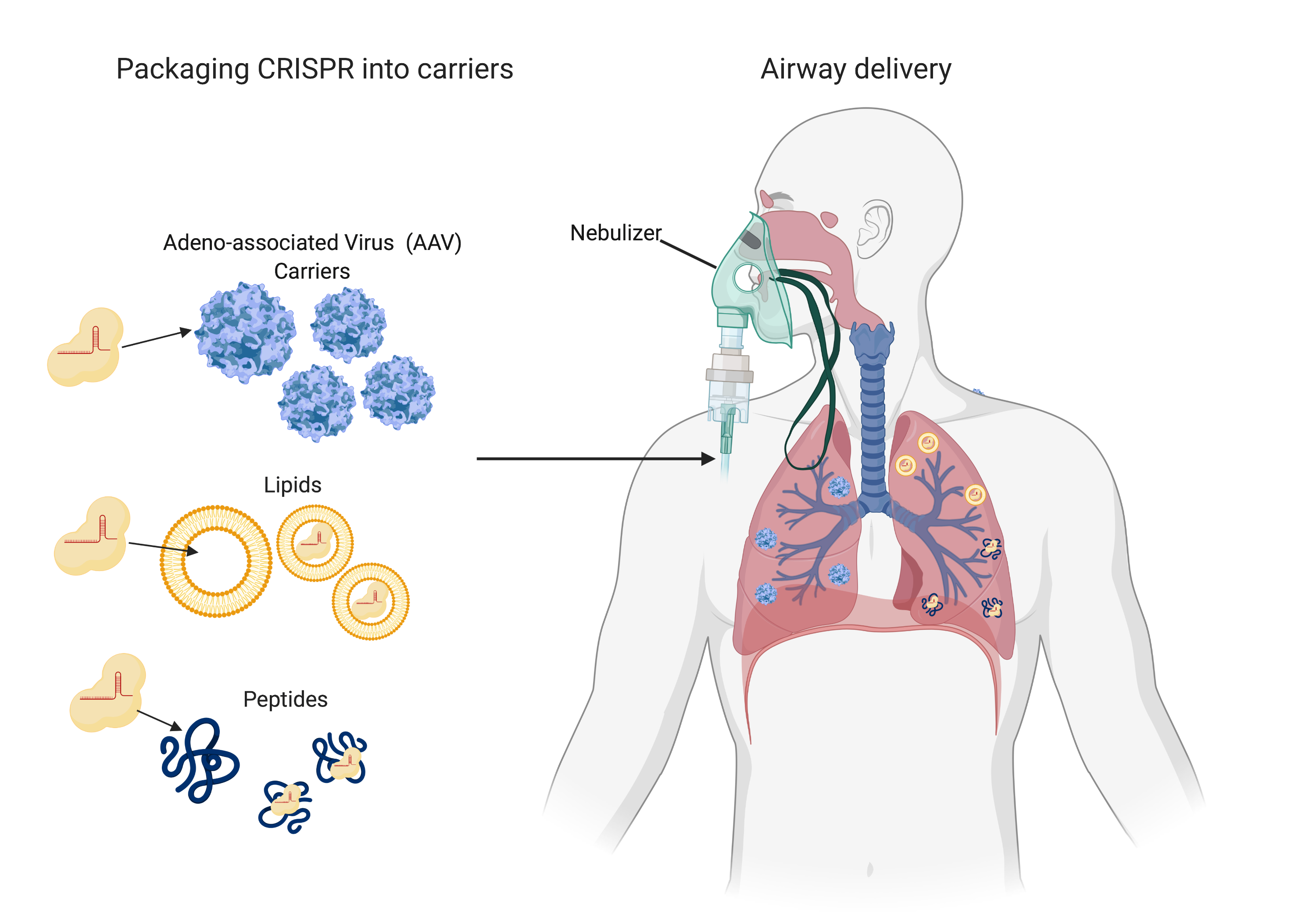
ومن قبيل التحذير، تقدم هذه الدراسات فقط دليلاً على استراتيجيتها التصورية والمفهومية، ولا يزال أمامها طريق طويل، حيث لم يطوّر العلماء بعد نظامًا لتطبيق كريسبر على خلايا الرئتين لدى المرضى. وقد أظهر فريق الدكتور باندولفي أنه يمكن تجميع كريسبر في جزيئات فيروسية فارغة (ناقلات فيروس الغدة المرتبطة) في نهج يُعرف بـ"فيروس في مواجهة فيروس".
وتدخل ناقلات فيروس الغدة المرتبطة الخلايا بنفس الطريقة التي يستخدمها فيروس كورونا، حيث تطلق هذه الناقلات كريسبر للعثور على الحمض النووي الريبوزي الفيروسي وتدميره. ويخطط فريق الدكتور ستانلي كي لاستخدام ناقلات تتكون من الدهون أو الببتيدات لتغليف كريسبر. وبعد ذلك، يمكن إعطاء هذه الناقلات للمرضى من خلال نظام البخاخات أو بخاخات الأنف كعلاج مضاد للفيروسات. ولا يزال هناك حاجة لاختبار هذه الأنظمة على الحيوانات من أجل ضمان سلامتها وفاعليتها، ومع المرضى لتعديل معايير الجرعة، وهي عملية قد تستغرق سنوات على الأرجح. وعلى الرغم من أننا قد لا نرى كريسبر يكافح كوفيد-19، فقد يكون جاهزًا تمامًا عند ظهور فيروس آخر جديد.
استخدام كريسبر في تشخيص كوفيد-19
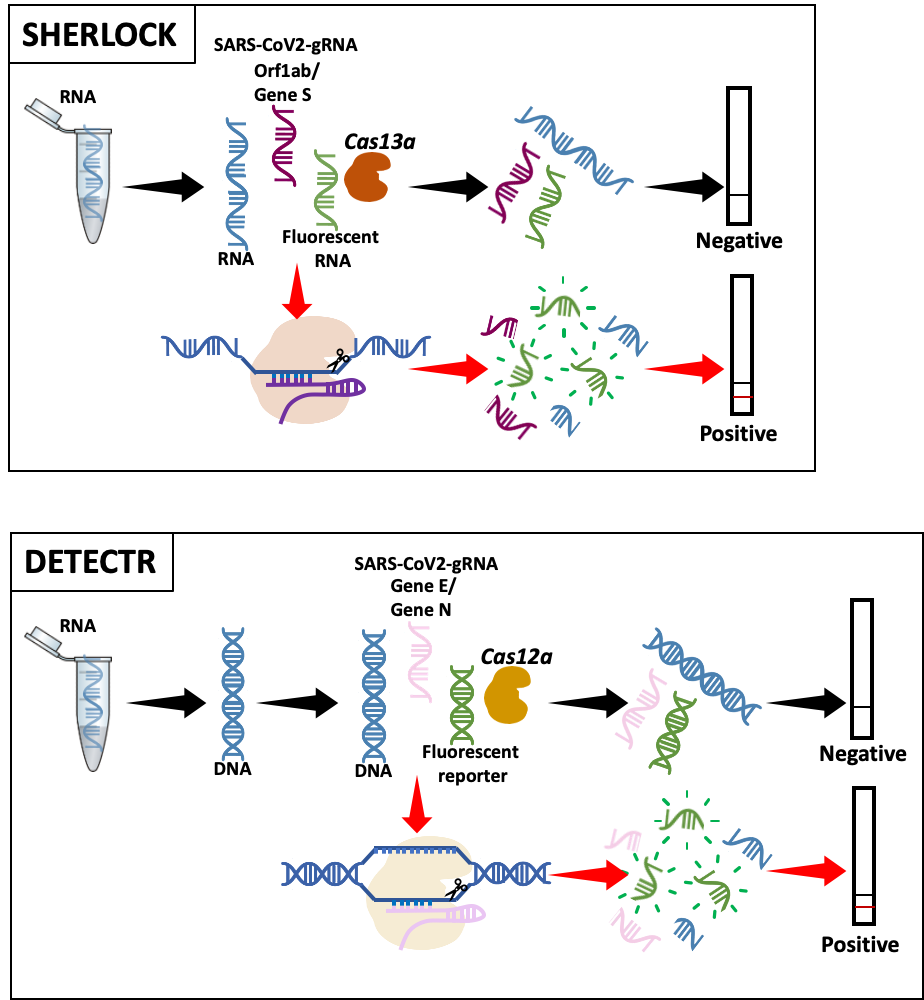
يمكن تطبيق نظام (CRISPR-Cas) ليس فقط لتعديل الجينوم وعلاجه، ولكن أيضًا لتشخيص الأمراض. ففي عام 2018، نشر رواد تعديل الجينات ورقتين بحثيتين متوازيتين تصفان المنصات القائمة على كريسبر للاكتشاف السريع للفيروسات أو الحمض النووي لخلايا الورم. وطور مختبر (Zhang) النهج الأول المسمى بناقل الإغلاق ذي الحساسية الإنزيمية العالية "SHERLOCK"، في "معهد برود" للطب الحيوي والجينات في الولايات المتحدة الأمريكية. وبعد توصيف جينوم فيروس كورونا، قاموا بتكييف نهج ناقل الإغلاق ذي الحساسية الإنزيمية العالية بهدف اكتشاف فيروس كوفيد-19.
بإيجاز، يرتبط الحمض النووي الريبوزي الموجه، وهو المصمم للكشف عن فيروس (Orf1ab) أو جين (S)، بالمتتالية المستهدفة، وينشط إنزيم (Cas13a)، الذي يعمل على حل الحمض النووي الريبوزي، حيث يتم تضمين الحمض النووي الريبوزي المصنف في الاختبار لتوليد إشارة قابلة للكشف، تشير إلى أن إنزيم (Cas) نشط وأن العينة "إيجابية". وفي الوقت الحالي، تستخدم هذه الطريقة للأغراض البحثية فقط.
أما التقنية الثانية وهي ناقل نيدوكلازات الحمض النووي عبر كريسبر، المعرفة اختصارًا بـ"الكاشف"، فقد بدأ تطويرها في مختبر (Doudna Lab) في جامعة كاليفورنيا في بيركلي للكشف عن الحمض النووي. وقد جرى تعديله مؤخرًا لاكتشاف كوفيد-19. والإنزيمات المستخدمة هي (Cas12a) و(gRNAs) مصممة إما للكشف عن جين (N) أو جين (E). ويتم تصور الاكتشاف على طريقة (SHERLOCK). وقد تم التحقق من صحة هذا النهج من خلال عينات المرضى، على الرغم من أن إدارة الغذاء والدواء الأمريكية لم توافق عليه بعد.
تكمن الميزة الرئيسية لتشخيص كوفيد-19 استنادًا إلى كريسبر في سهولة وسرعة استخدامه في معظم المختبرات. ومع ذلك، فإن دقه الاختبار تعتبر أقل مقارنة بمعيار (qRT-PCR)، وهو ما يسمى بتفاعل البوليمراز التسلسلي اللحظي مع النسخ العكسي.
ويستخدم باحثون آخرون استراتيجيات مماثلة، ولكنها مُحسنة، للتغلب على هذا العائق، ولكن الدراسات لا تزال في بدايتها. على سبيل المثال، تم تصميم (AIOD-CRISPR)، باستخدام جزيئين من (gRNA) لزيادة نوعيته وتحقيق جميع الخطوات في أنبوب اختبار واحد، وكذلك اختبار (CREST)، وهو إجراء فعال من حيث التكلفة يجمع بين قوة اختبار تفاعل البوليمراز التسلسلي (PCR) مع الاكتشاف القائم على كريسبر.
المشاركون في هذه الدراسة:
تقنية كريسبر وعلاج كوفيد-19 بكريسبر: كريم شلبي ود. فيجاي جوبتا
تشخيص كوفيد-19 بكريسبر: د. سلام سلوم أصفار
الرسوم التوضيحية: كريم شلبي ود. فيجاي جوبتا ود. سلام سلوم أصفار
مراجعة النص العربي واعتماده: د. نور مجبور
المحررون: د. أدفيتي نايك ود. ألكسندرا بتلر
لتصفح المراجع، يُرجى الضغط هنا.




